S28 Het Aufbau-principe
Aim: To explain the Aufbau principle and determine the electronic configuration. |
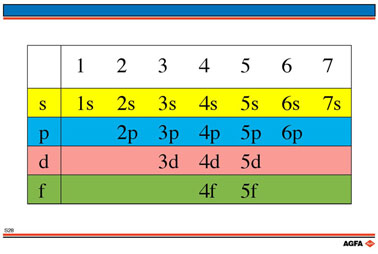
Deze illustratie
wordt het best getoond zonder gebruik te maken van de overlegillustratie
S1.
De leerkracht kan tijdens de les de pijltjes aanduiden op de illustraties
zoals hiernaast voorgesteld.
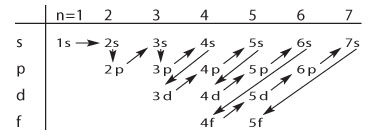
Deze opvulmethode werd voor het
eerst voorgesteld door Wolfgang Pauli (1900-1958).
De elektronen worden opgevuld volgens stijgend orbitaalenergieniveau.
Al de orbitalen van een bepaalde schil en subschil hebben dezelfde energie.
Voor een gegeven waarde van n stijgt de energie van
s -> p -> d -> f.
Bij hogere energieniveaus kan
het in zeldzame gevallen voorkomen dat het Aufbau-principe niet gevolgd
wordt:
bv. Ac: 7s2
6d1 i.p.v. 7s2 5f1:
de energieniveaus van verschillende schillen overlappen elkaar.
Referentie:
R. H. Petrucci and W. S. Harwood, General Chemistry, Principles and Modern Applications,
Macmillan, New York (1989).