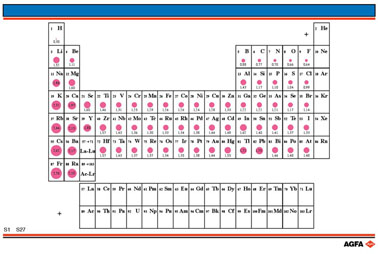
S27 Atoomstralen (atoomradii)
|
Doel : Een idee geven van hoe de grootte van de atomen varieert als functie van hun plaats in het periodiek systeem. |
Er zijn verschillende manieren om de grootte van atomen weer te geven of om hun relatieve grootte te bepalen. De covalente atoomstraal wordt gedefinieerd als de halve afstand tussen het middelpunt van de kernen van twee identieke atomen, wanneer die in een enkelvoudige covalente binding verenigd zijn.
De getallen zijn de waarden in
Angström (10-10 m).
De cirkels geven een relatief visueel beeld van de atoomgrootte (1).
Men kan de volgende structuur herkennen : in het periodiek systeem stijgt
de atoomradius in een groep van boven naar onder. In een periode daalt
ze van links naar rechts.
Referentie:
1) H.F. Holtzclaw and W.R. Robinson, College Chemistry, D. C. Heath and
Company Lexington, (1988)