ST09
Scheiding van homogene vast-vloeibaarmengsels
|
Doel : het tonen van twee kristallisatieprocessen op respectievelijk
laboratorium- en industriële schaal. |
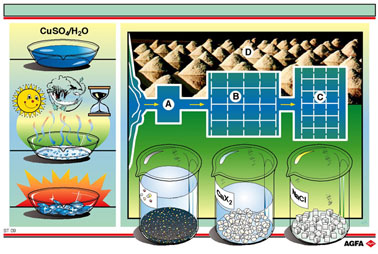
Links op de illustratie ST09 wordt het uitkristalliseren van een waterige
kopersulfaatoplossing getoond. Bij het langzaam verdampen van het water
worden mooie blauwe kopersulfaatkristallen gevormd. Hierdoor wordt uit
de homogene oplossing kopersulfaat gescheiden van het oplosmiddel.
Rechts op de illustratie wordt de winning van zout uit zeewater getoond.
Een proces dat o.a. in verschillende Zuid-Europese landen nog frequent
wordt toegepast. Het zeewater wordt via een sluis in een eerste bezinkingsbekken
(A) gebracht. Hier bezinken zand en slib. Het geklaarde zeewater wordt
via sluizen in een eerste kristalliseerpan (B) gebracht. Hier slaan de
minder en weinig oplosbare calciumzouten neer (o.a. de calciumhalogeniden).
Vermits hier reeds een gedeeltelijke verdamping van het water plaatsgrijpt,
stijgt de concentratie van het natriumchloride.
Wanneer het
oorspronkelijke volume tot ongeveer 1/10 is gedaald, wordt de bijna verzadigde
zoutoplossing via sluizen overgebracht naar de ondiepe zouttafels (C).
Hier kristalliseert keukenzout (NaCl) uit door het snel verdampen van
het water. Het uitgekristalliseerde zout wordt vervolgens op hopen geschept
(D).