T08 Le Troisième Principe de la thermodynamique
But: Illustrer le Troisième Principe de la Thermodynamique. |
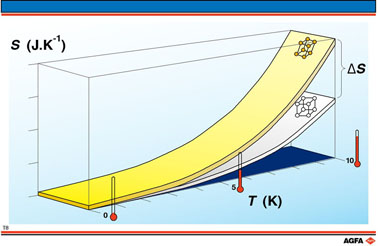
La transformation physique d'une matière chimique (p.ex. le soufre) de situation A (rhombique) en situation B (monoclinique) à une température normale est accompagnée d'un changement d'entropie. Par des expériences, on a établi qu'à mesure qu'on s'approche de la température 0 K, le changement d'entropie dans la transformation diminue.
Etant donné que 0 K ne peut jamais être atteint, on établit que:
lim DS
= 0
T ® 0
De manière
intuitive, on peut comprendre ce Troisième Principe en partant de l'idée
que le mouvement atomaire, moléculaire ou ionique, qui est un degré pour
indiquer le désordre et donc l'entropie, cesse complètement au zéro absolu.
De ce fait, il n'y aura pas de changement de désordre ou d'entropie lors
de transformations physiques ou chimiques à 0 K.