T04
Le Deuxième Principe de la thermodynamique
|
But: Illustrer le Deuxième Principe de la thermodynamique
- définition du changement d'entropie. |
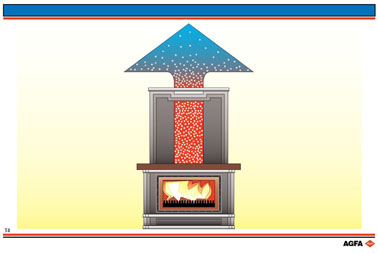
Des gaz
chauds dans une cheminée se répandent dans l'environnement
et se mêlent aux gaz environnants.
De ce fait, les gaz chauds de la cheminée se refroidissent tandis
que les gaz environnants se réchauffent: la chaleur se diffuse
spontanément.
Le phénomène inverse, c.-à-d. une diffusion spontanée
de gaz chauds dans la cheminée provenant de l'extérieur,
est impossible.
Le Deuxième
Principe décrit en quelle direction un processus ou un phénomène
a lieu. Intuitivement, nous savons que le flux de chaleur est à
sens unique: du chaud au froid.
Mathématiquement, ce phénomène est décrit
par les notions d'entropie et de changement d'entropie.
L'entropie
(S) est une fonction qui décrit une situation.
Le changement d'entropie (DS)
décrit donc le passage d'une situation à une autre.
Le changement d'entropie dans un processus est défini comme la
chaleur échangée (DQ)
divisée par la température absolue (T):
![]()
Dans un système isolé, le changement d'entropie DS
> 0
Puisque le Premier Principe nous apprend que les changements en quantité
de chaleur sont identiques, et puisque la température absolue du
gaz chaud est supérieure à celle du gaz froid, l'équation
ci-dessus nous montre que S est positif quand le gaz chaud cède
de la chaleur (le changement de chaleur est négatif).
DS
= 0 quand les deux températures sont égales, donc quand
le système est en équilibre.
Ceci ne veut pas dire que l'entropie d'un système ne peut pas baisser, mais il s'agit dans ce cas d'une action forcée. Ces processus ne peuvent se manifester que lorsequ'on ajoute au système precis de l'énergie venant de l'extérieur, c.-à-d. lors d'un système non isolé.
Conseil:
Illustrer
le Deuxième Principe par le mélange d'eau chaude et froide
dans un bain.
Quand on ajoute de l'eau chaude à un bain qui est partiellement
rempli d'eau froide, l'eau chaude se mêlera spontanément
à l'eau froide. De ce fait l'eau chaude se refroidit et l'eau froide
se réchauffe jusqu'à ce que la température désirée
soit atteinte. Le phénomène inverse est impossible c.-à-d.
la séparation de l'eau à la temperature désireé
en une flaque d'eau froide et chaude .