C05 Un système colloïdal pratique: la "mayonnaise"
But: Montrer que bien des substances de la vie quotidienne sont en fait des systèmes colloïdaux compliqués. |
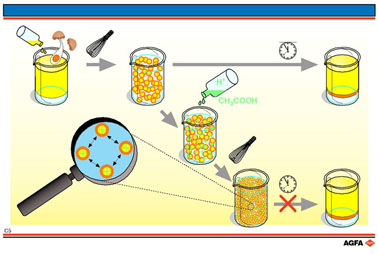
Pour la préparation
culinaire de la mayonnaise on part d'un jaune d'oeuf, de vinaigre, de
poivre et de sel. On y ajoute de l'huile que l'on disperse en très fines
gouttelettes d'un diamètre de l'ordre du micron. Ceci a lieu par l'effet
mécanique d'un fouet manié par la main. Un tel système où la phase dispersée
(l'huile) et continue (jaune d'oeuf et acide acétique dilué) sont toutes
deux liquides, s'appelle une émulsion. Dans ce cas il s'agit d'une émulsion
de l'huile dans l'eau (émulsion huile/eau).
L'acide acétique dilué est ajouté pour le goût et modifie aussi le degré d'acidité (pH). Ceci peut avoir une influence sur les charges des protéines et altérer l'action stabilisante de ces dernières.