T08 De derde hoofdwet van de thermodynamica
|
Doel : Illustreren van de derde hoofdwet van de thermodynamica. |
De
derde wet van de thermodynamica stelt dat bij fysische of chemische omzettingen
tussen zuivere stoffen bij het absolute nulpunt (T=0 K), de verandering
in entropie DS
nul is.
De
fysische omzetting van een chemische stof (vb. zwavel) van toestand A
(rombisch) in toestand B (monoclien) bij normale temperatuur gaat gepaard
met een verandering in entropie.
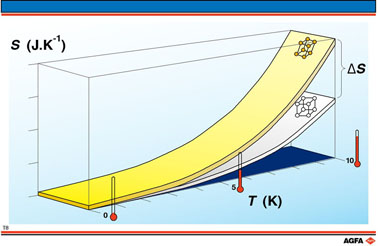
Experimenteel stelt men vast dat naarmate de temperatuur 0 K nadert, de
omzetting gepaard gaat met een dalende entropieverandering.
Daar 0 K niet bereikt kan worden, stelt men dat :
lim DSt
= 0
T ® 0
Intuïtief kan deze derde hoofdwet begrepen worden door te bedenken
dat de atomaire, moleculaire of ionaire beweging die een maat is voor
de wanorde en dus voor de entropie, bij het absolute nulpunt volledig
stilvalt. Hierdoor zal er bij een fysische of chemische omzetting bij
0 K geen verandering zijn in wanorde en dus ook niet in entropie.