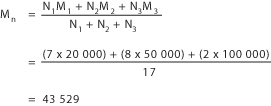POL03: La distribution des masses moléculaires - la polydispersité
|
Obj.: Illustrer la polydispersité d’un échantillon polymère et déterminer la masse moléculaire moyenne en nombre |
Par la séparation en GPC, on obtient trois fractions,
à partir desquelles on peut alors déterminer la distribution des masses
moléculaires des polymères. Même après la séparation, les fractions sont
encore constituées par des molécules polymères de grandeurs variables.
Sur l'illustration POL 03-A, on représente un exemple de séparation. On
ne peut calculer que des valeurs statistiques de la masse moléculaire.
A ce stade de la présentation, il nous faut introduire l’expression
“ degré de polymérisation ” (DP). Le DP fournit le nombre de
constituants (monomères) dont est composée une molécule polymère.
Sur l'illustration POL 03-A, la courbe en rouge représente la distribution globale dans laquelle sont additionnées toutes les fractions: WX (%) représente le pourcentage en poids de chaque fraction.
Pour se faire une idée de la polydispersité d’un polymère, on sélectionne pour le DP des valeurs arbitraires à partir de valeurs connues pour la masse moléculaire du monomère et pour le nombre de molécules de chaque espèce. Il s’agit d’une approximation simplifiée. Celle-ci a été sélectionnée dans le but d’expliquer le raisonnement suivi lors de la détermination d’une masse moléculaire moyenne. En réalité, le nombre des molécules est de loin supérieur.
Ainsi, on
peut construire une courbe qui laisse apparaître la polydispersité.
A cet effet, on extrait le pourcentage en poids des différentes entités
présentes dans les trois fractions en fonction du DP. Cette façon de procéder
est illustrée sur l'illustration POL 03-B.
En fonction du procédé de mesure que l’on a suivi, les masses moléculaires peuvent être représentées par différentes valeurs moyennes. En l’occurrence, on choisit la valeur moyenne en nombre que l’on obtient par exemple à partir de mesures de la pression osmotique, de l’analyse des groupes terminaux ou encore de mesures de la pression de vapeur. Cette valeur est fournie par la formule:
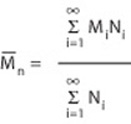
Mi
représente la masse moléculaire de l’espèce i et Ni représente
le nombre de molécules de l’espèce i.
Dans l’exemple choisi, on utilise un monomère (fictif) possédant
une masse moléculaire égale à 10. Les degrés de polymérisation respectifs
pour les trois fractions sont désignés ci-dessous par les lettres X, Y
et Z .
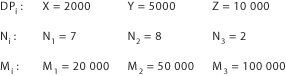
A partir de là, on calcule facilement les fractions pondérales représentées sur l'illustration POL 03-B (19%, 54%, 27%). La fraction pondérale de l’espèce i=1 est calculée comme suit:

Dans cet exemple simplifié, la masse moléculaire moyenne en nombre est égale à: