T11 Processus spontanés et forcés
But: Illustrer des processus impossibles et naturels. |
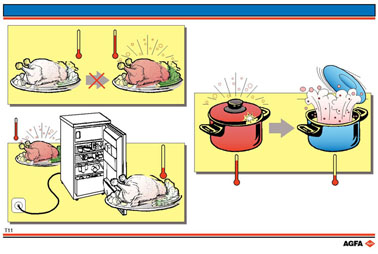
Une casserole
ne se réchauffe pas spontanément.
Le transfert de chaleur d'un milieu froid vers un corps chaud est impossible.
Si le mouvement de la chaleur s'effectuait dans cette direction, et si
la quantité de chaleur cédée par le milieu froid était égale à celle absorbée
par le corps chaud, l'entropie perdue dans le milieu froid serait supérieure
à celle acquise par le corps chaud.
Une marmite chaude cède de la chaleur à l'environnement et peut faire danser son couvercle.
Le
flux de chaleur s'effectue de la marmite chaude vers l'environnement froid.
De ce fait, l'accroissement de l'entropie dans le milieu extérieur est
supérieur à la diminution de l'entropie dans la marmite. L'entropie du
système accroît, même si l'environnement froid ne peut qu'absorbée partiellement
cette chaleur . Le reste du transfert d'énergie est disponible pour le
travail,ce qui s'appelle énergie libre. Ce principe explique le fonctionnement
de la machine à vapeur.
Le fonctionnement d'un frigo n'est pas un processus contre nature. Dans
le frigo, la température est basse parce que la chaleur du frigo est déviée
vers l'environnement plus chaud.
Un
flux de chaleur allant du froid au chaud mènerait à une baisse de l'entropie,
et ne peut se manifester que quand il y a de la chaleur supplémentaire
qui se dégage dans l'environnement chaud.
Cette chaleur supplémentaire est fournie par un moteur électrique qui
actionne le frigo. Pour ce faire, de l'énergie (électrique) supplémentaire
est ajoutée au système.