H04 - H05 La dissolution d'un cristal de sel dans l'eau
|
But: Visualiser le processus de solubilisation et d'hydratation de NaCl. |
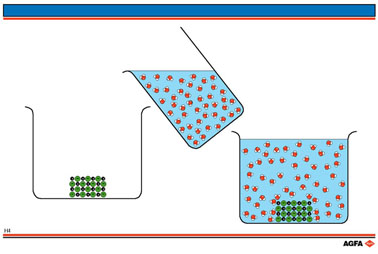
Les illustrations H4 et H5 montrent les étapes successives de solubilisation et d'hydratation d'un cristal de NaCl.
On part d'un
cristal cubique auquel est ajoutée de l'eau. Le caractère bipolaire des
molécules d'eau les oriente autour du cristal.
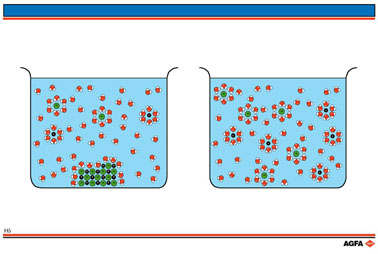
Les ions sodium (Na+) attirent plus particulièrement les atomes d'oxygène, les ions chlorure (Cl-) s'entourent des hydrogènes.
Les ions sont ensuite hydratés et chacun reçoit un manteau d'eau, ou hydrate dans lequel l'orientation des molécules d'eau est déterminée par leurs charges.
Finalement, le cristal est entièrement dissous.