S28 Le principe d'exclusion
But: Expliquer le principe d'exclusion. Déterminer la structure électronique. |
Il est souhaitable que cette illustration soit montré sans que l'illustration S1 soit superposé.
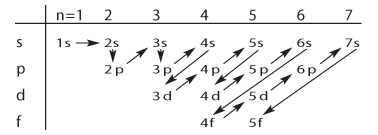
Cette méthode de remplissage a été proposée pour la première fois par
Wolfgang Pauli (1900-1958).
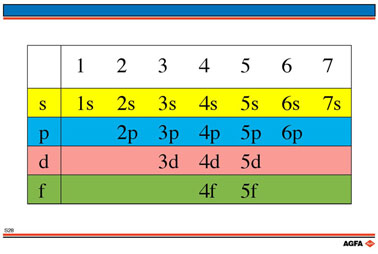
Les électrons sont remplis en fonction du niveau d'énergie orbitale croissant.
Toutes les orbitales d'une certaine couche et sous-couche ont la même
énergie. Pour une valeur donnée n l'énergie augmente de
s ->p ->d ->f.
Pour les niveaux d'énergie plus élevés, il arrive, mais c'est rare, que
le principe d'exclusion ne soit pas suivi.
p.ex. Ac: 7s2 6d1 au lieu de 7s2 5f1:
les niveaux d'énergie de couches différentes se recoupent.
Référence:
C.E. Mortimer, Chemistry, Wadsworth Publishing Company, Belmont, California.