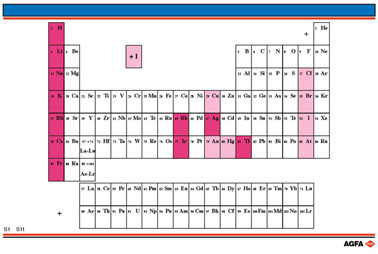
S11 - S22 Les nombres d'oxydation
|
But: Présenter les nombres d'oxydation principaux des éléments. |
Les 12 illustrations
superposables (S11 - S22) sont tous construits sur le même modèle. Le rouge (positif) ou
le bleu (négatif) est utilisé suivant le signe du nombre d'oxydation.
Ceci a, par exemple, pour conséquence que les groupes Ia et IIa peuvent clairement être projetés comme des colonnes +I et +II, mais que pour être complet et scientifiquement correct le nombre d'oxydation -I doit également figurer avec une coloration plus légère chez les halogènes.
Aucun nombre
d'oxydation n'est donné pour les lanthanides et les actinides ni, pour
des raisons didactiques, pour les gaz rares (bien que Kr, Xe et Rn peuvent
former des composés).
Pour des métaux particuliers (V, Cr, Mn, Fe, Co, Ni, Mo, Ru, Rh, Pd, W,
Os, Ir et Pt), le nombre d'oxydation peut être zéro; ceci n'est pas indiqué.
Pour être complet, il faut signaler que quatre métaux peuvent présenter le nombre d'oxydation -I (Mn, Co, Re et Ir) et que Fe, Ru et Os peuvent même présenter le nombre d'oxydation -II. Ceci n'est pas montré dans l'illustration.
Référence:
L'information complète peut être trouvée dans le tableau périodique des
éléments publié par le JVCV en avril 1989 en annexe à la revue Elektron
(vol. 3, n° 3).